Fusiones RSPO3 vinculadas a menor supervivencia en CCR avanzado
Qué es el cribado genético de portadores, a quién indicarlo y cómo integrarlo con los test CIDEGEN 511-00145/46/47/48.
CAR-T frente a tumores HER2+: estado del arte y cómo integrarlo con el diagnóstico molecular
Qué sabemos de las CAR-T dirigidas a HER2 en tumores sólidos y cómo integrar HER2 (IHQ/FISH/NGS) en la ruta asistencial.
Células NK contra el cáncer de pulmón agresivo: ¿qué aporta la inmunoterapia innata?
Avances con células NK en cáncer de pulmón y cómo integrar el Panel 60-00026 de CIDEGEN en la ruta diagnóstica.
Revumenib aprobado por FDA para LMA R/R con mutación NPM1
Qué es la enfermedad de Huntington, cómo se diagnostica (expansión CAG en HTT) y recomendaciones prácticas para la vía asistencial.
Cáncer de mama triple negativo: dianas terapéuticas y decisión clínica
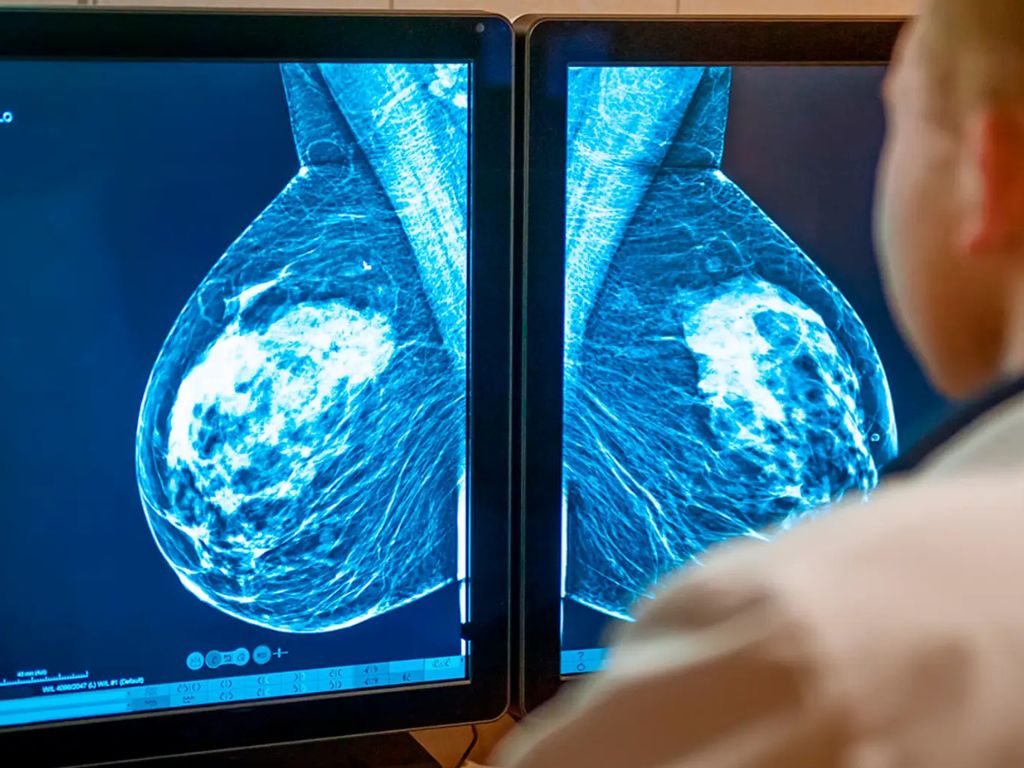
El cáncer de mama triple negativo (TNBC) representa ~10–15% de los tumores mamarios y se caracteriza por ausencia de RE/RP y de amplificación de HER2. Es biológicamente heterogéneo y con mayor agresividad clínica.
Linfoma: qué medir hoy para decidir tratamiento

El diagnóstico moderno del linfoma requiere integrar múltiples técnicas. En CIDEGEN ofrecemos el Perfil Linfoma (Ref. 60-00015), un panel multi-técnica diseñado para apoyar la práctica clínica y anatomopatológica.
ESR1 en cáncer de mama metastásico: cuándo y cómo testear
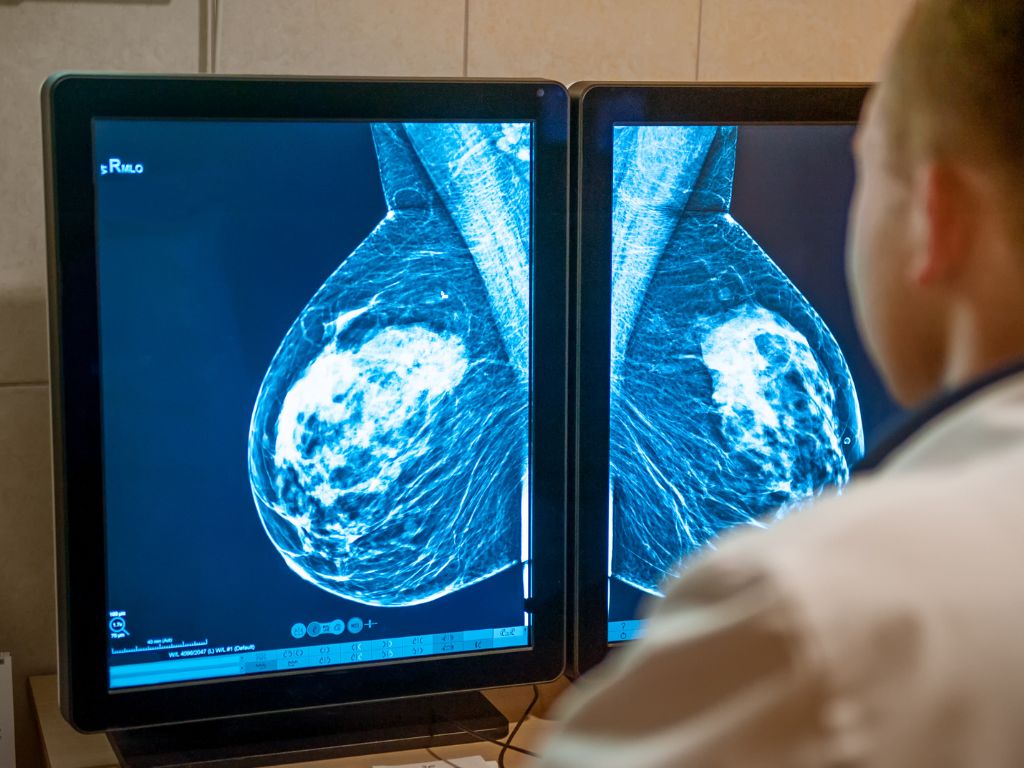
ASCO recomienda testear ESR1 en cáncer de mama HR+/HER2− metastásico al progresar con terapia endocrina. ¿Cuándo, cómo y con qué impacto clínico?
Elacestrant y mutación ESR1 en cáncer de mama avanzado
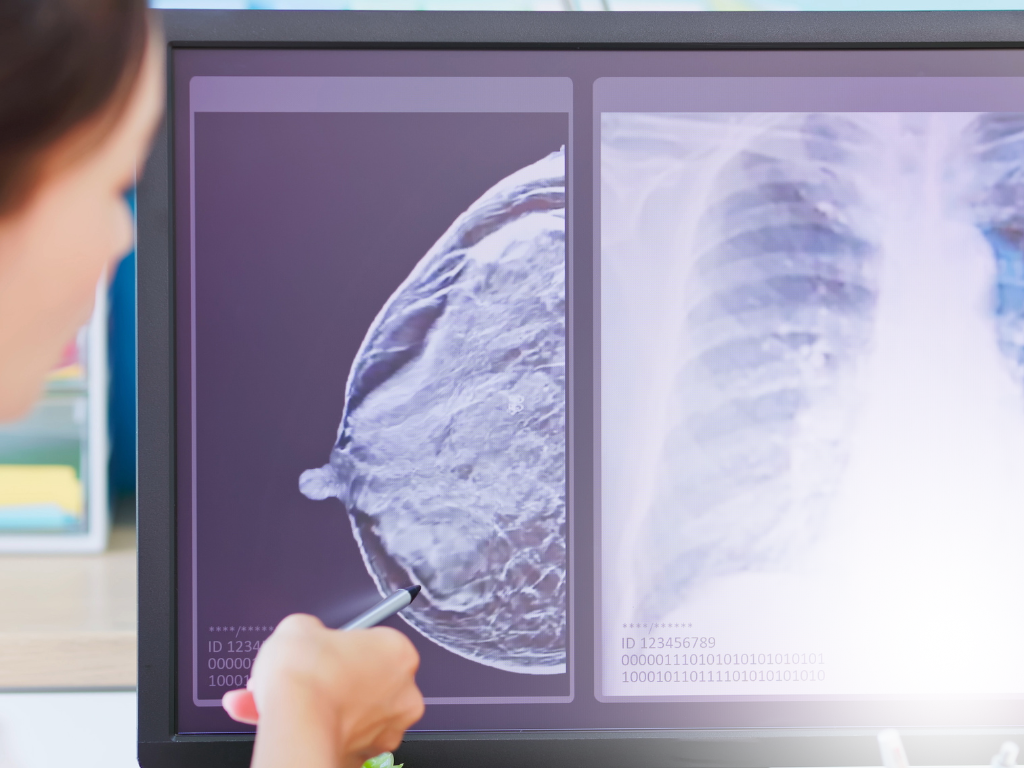
Elacestrant, primer SERD oral aprobado, ha mostrado beneficio significativo en cáncer de mama RE+/HER2− con mutación ESR1. En CIDEGEN ofrecemos el diagnóstico de ESR1 por NGS en plasma o tejido para apoyar decisiones terapéuticas de precisión.
Nuevos avances en cáncer de próstata metastásico: combinación de enzalutamida y talazoparib mejora la supervivencia

Un estudio internacional muestra que combinar enzalutamida con talazoparib prolonga la supervivencia libre de progresión en pacientes con cáncer de próstata metastásico resistente a la castración con alteraciones en genes de reparación del ADN, consolidando el papel de la oncología de precisión.
Análisis de la Vía HRD y su Impacto en la Terapia Personalizada en Oncología

La Deficiencia en la Reparación por Recombinación Homóloga (HRD) es un biomarcador clave en oncología de precisión, ya que permite predecir la respuesta a inhibidores PARP y a quimioterapias basadas en platino.
